کلروفرم همچنین به عنوان تری کلرومتان و متیل تری کلراید شناخته می شود، یک ترکیب شیمیایی و از خانواده حلال ها است. در دمای اتاق، یک مایع بی رنگ است که فرار اما غیر قابل اشتعال است. یک حلال بسیار مؤثر برای ترکیبات مختلف آلی است که در تحقیقات اصلی و فرآیندهای صنعتی مورد استفاده قرار می گیرد. این ماده برای واکنش های شیمیایی خاص یک معرف می باشد.
با این حال کلروفرم باید با احتیاط مصرف شود، زیرا هم برای سلامتی انسان و هم برای محیط زیست مضر است. استنشاق بخارات آن باعث تحریک سیستم عصبی مرکزی می شود و می تواند باعث سرگیجه، خستگی و سردرد شود. قرار گرفتن در معرض مزمن ممکن است به کبد و کلیه ها آسیب برساند و برخی از افراد نسبت به آن واکنش آلرژیک دارند.
خواص و مشخصات شناسایی کلروفرم
| خواص | مشخصات |
| دانسیته (در۰C 25) (g/ml) 1/492 | فرمول شیمیایی CHCl۳ |
| نقطه ذوب (۰C) 63- | وزن مولکولی (g/mol) 119/38 |
| حلالیت درآب (در ۰C20) (g/100ml) 0/809 | شماره (CAS No) 67-66-3 |
| اسیدیته (pka) ۱۰/۴ | نام های دیگر: تری کلرومتان، متیل تری کلراید |
انواع فرایندهای تولید کلروفرم
فرایندهای زیادی برای تولید کلروفرم وجود دارد، که عبارتند از:
۱)کلر زنی متان
در واکنش کلرزنی متان می توان دامنه عملکرد را از ۹۰ تا ۹۵ درصد نشان داد، اما استفاده از راکتورهای بستر ثابت مستلزم ساخت کانسیلر ساخته شده است تا به اندازه کافی قوی برای پشتیبانی از کاتالیزور باشد.
۲) کلرزنی فتوشیمیایی
بازده ۹۰٪ خواهد بود و این واکنش می تواند ناخالصی ها کلرومتان حاصل را کاهش دهد، اما ظرفیت هر راکتور بسیار کم است، بنابراین واکنش های کند را داریم.
۳) واکنش بین استون و کلرین
۲CH۳COCH۳ (l) + ۶ CaOCl۲.H۲O (s) → ۲CHCl3 (l) + Ca (CH۳COO) ۲ (s) + ۲Ca (OH) ۲ (s) +۳CaCl۲ (s) + ۶ H2O (L)
این واکنش تولید کلروفرم خام در راکتورهای دسته ای است و با فرآیند تخریب خالص سازی خواهد شد. بازده این واکنش ۸۶ تا ۹۱ درصد است. اما این روند شامل یک فرایند متعارف است. بنابراین برای تولید کلروفرم در شرایط بهینه، واکنش بین استون و کلرین انجام می شود.
طیف IR حالت گازی کلروفرم
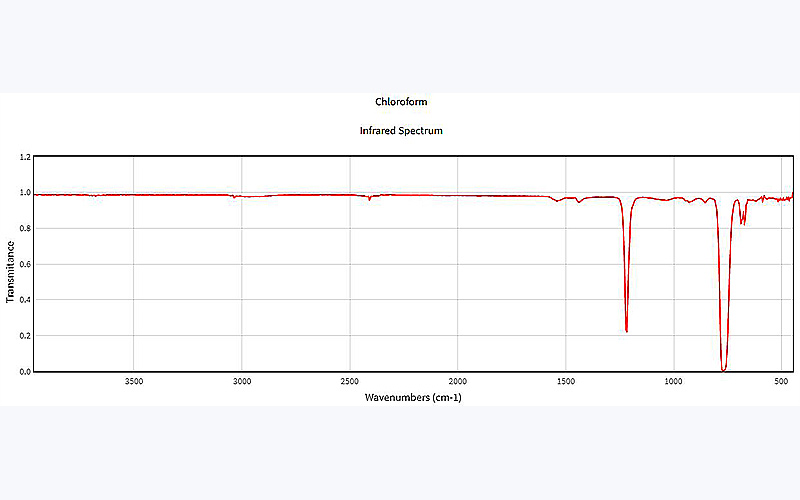
کاربرد کلروفروم در صنایع

تا همین اواخر، کلروفرم به طور عمده برای تولید مبرد فرنی R-22 مورد استفاده قرار گرفته است. این استفاده، در حال کاهش است، زیرا پروتکل مونترال به اجرا در می آید و R-22 با مبرد هایی جایگزین می شود که نقش کمتری در بین رفتن ازن را داشته باشند.
مقادیر کمتری از کلروفرم به عنوان یک حلال در صنعت داروسازی و برای تولید رنگها و سموم دفع آفات استفاده می شود. به عنوان یک حلال برای تحقیق در آزمایشگاه های شیمی دانشگاهی استفاده می شود.
به عنوان یک حلال می توان از آن برای اتصال قطعات شیشه اکریلیک (تحت نام تجاری “Perspex”) استفاده کرد. کلروفرم برای شکل گیری پایه موثرترین حلال برای آلکالوئیدها است و از این رو برای استخراج مواد گیاهی برای فرآوری دارویی استفاده می شود.
به عنوان مثال، از این تجارت برای استخراج مورفین از خشخاش ها، اسکوپولامین از گیاهان Datura استفاده می شود. غالباً در حضور یک بافر استخراج، برای جدا کردن DNA از مواد سلولی دیگر استفاده می شود. DNA به درون ماده طبیعی می رود، در حالی که پروتئین و مواد سلولی نامحلول بین لایه های بافر و کلروفرم رسوب می کنند. کلروفرم حاوی دوتریوم (هیدروژن سنگین)، CDCl۳، یک حلال رایج است که در طیف سنجی NMR مورد استفاده قرار می گیرد.
سمیت کلروفروم
همانطور که از آن به عنوان ماده بیهوشی استفاده می گردد، اما استنشاق بخارات کلروفرم باعث سرکوب سیستم عصبی مرکزی می شود. تنفس حدود ۹۰۰ قسمت کلروفرم به ازای هر میلیون قطعه هوا (۹۰۰ قطعه در میلیون) برای مدت زمان کوتاه می تواند باعث سرگیجه، خستگی و سردرد شود.
قرار گرفتن در معرض مزمن کلروفرم ممکن است باعث آسیب به کبد (جایی که کلروفرم به فسژن متابولیزه می شود) و کلیه ها می شود و بعضی از افراد هنگام تماس پوست شان در کلروفرم دچار زخم می شوند.
تقریباً ۱۰ درصد از جمعیت دارای واکنش آلرژیک نسبت به کلروفرم هستند که قرار گرفتن در معرض آن، تب حدود ۴۰ درجه سانتیگراد (۱۰۴ درجه فارنهایت) ایجاد می کند. مطالعات حیوانات نشان داده است که سقط جنین در موش ها و موش هایی که در طول بارداری هوای حاوی ۳۰ تا ۳۰۰ ppm کلروفرم و همچنین در موش هایی که کلروفرم در دوران بارداری خورده اند یا تنفس شده است رخ می دهد.
کلروفرم زمانی در خمیردندان ها، شربت های سرفه، پمادها و سایر داروها ظاهر می شد، اما از سال ۱۹۷۶ در محصولات مصرفی در ایالات متحده ممنوع شده است. گزارش یازدهم NTP در مورد سرطان زاها نشان می دهد که آن را به عنوان یک عامل سرطان زای انسانی پیش بینی می شود.
در حین ذخیره طولانی مدت، مقادیر خطرناک فسژن می تواند در حضور اکسیژن و نور ماوراء بنفش جمع شود. برای جلوگیری از حواذث، کلروفرم تجاری با اتانول یا آمیلن تثبیت می شوند، اما نمونه هایی که بازیابی شده اند یا خشک شده اند دیگر حاوی هیچ گونه تثبیت کننده ای نیستند و باید با آن ها احتیاط کرد.


بدون دیدگاه